Technische Daten des Accu-Chek SmartGuide Geräts
Produktname
Accu-Chek SmartGuide Gerät
Funktionsweise
Das Gerät besteht aus einem Applikator und einem Sensor. Der Applikator wird nach dem Anbringen des Sensors entsorgt, während der Sensor auf der Haut des Benutzers verbleibt, wobei der elektrochemische Sensor in das Unterhautfettgewebe des Benutzers eingeführt ist. Der Sensor wird nach Ablauf seiner Tragezeit entsorgt.
Zur Kalibrierung des Sensors wird ein Glukosewert von einem Blutzuckermessgerät in die App eingegeben und anschließend an den Sensor gesendet. Um den Glukosespiegel kontinuierlich zu überwachen, werden die in der Gewebeflüssigkeit gemessenen Glukosedaten alle 5 Minuten vom Sensor an die App gesendet. Die App wird auf einem mobilen Endgerät ausgeführt.
Produktspezifikationen
Höhe (inkl. Pflaster) | 5,9 mm |
Länge der Nadel | 8,2 mm |
Durchmesser des Sensors ohne Pflaster | 33,3 mm |
Gewicht | 5 g |
Datenübertragung
Der Sensor überträgt folgende Daten an die App:
- Seriennummer
- Firmware-Version
- Hardware-Version
- Sensorinformationen (System-ID / MAC-Adresse)
- Zeit für die nächste Kalibrierung
- CGM-Werte
- Statusinformationen
CGM-Werte, die generiert werden, während sich der Sensor im Verlaufsmodus befindet, werden durch das Sensorstatus-Annunciation-Bit „Kalibrierung erforderlich“ angezeigt.
Der Sensor empfängt folgende Daten von der App:
- Blutzuckermesswert für die Kalibrierung
- Startzeit der CGM-Nutzungsdauer
Hochfrequenzsignale
Zweck der Schnittstelle | Kommunikationsschnittstelle. Ermöglicht den Austausch von Daten zwischen Sensor und mobilem Endgerät. |
Spezifikation der Schnittstelle | Bluetooth Low Energy 5.0 oder höher |
Frequenzband für Empfang und Übertragung von HF-Signalen | Frequenzband von BLE 5.0: 2,402–2,480 GHz |
Art und Frequenzcharakteristik der Modulation | Gaußsche Frequenzumtastung (Gaussian Frequency-Shift Keying, GFSK) |
Effektive Strahlungsleistung bei der Übertragung | weniger als 10 mW |
Methode zur Zeitsynchronisierung | Die Synchronisierung des Sensors erfolgt nach den Synchronisierungsintervallen des mobilen Endgeräts. |
Reichweite von Bluetooth Low Energy | 6 m |
Zugriff auf Verbindung mit mobilem Endgerät über Bluetooth Low Energy | Auf dem mobilen Endgerät muss Bluetooth Low Energy eingeschaltet sein, damit eine Verbindung hergestellt werden kann. |
Störung durch Hochfrequenzsignale | Die Kommunikation kann durch andere Hochfrequenzgeräte beeinträchtigt werden. |
Elektromagnetische Verträglichkeit (EMV)
Alle Tests zur elektromagnetischen Verträglichkeit wurden gemäß den Normen IEC 60601-1-2:2014 und IEC 60601-1-2:2014/AMD1:2020 durchgeführt.
Elektromagnetische Felder und elektromagnetische Strahlung können die Funktion des Sensors beeinträchtigen und zu falschen CGM-Werten führen. Wenn der Sensor nicht im Rahmen seiner technischen Spezifikationen verwendet wird, kann es zu Interferenzen mit anderen Geräten kommen (z. B. durch Bluetooth-Signale). Verwende den Sensor ausschließlich im Rahmen seiner technischen Spezifikationen.
Platziere keine anderen Geräte in der Nähe des Sensors oder auf dem Sensor. Bei der Verwendung des Sensors zusammen mit oder in der Nähe von anderen Geräten kann es zu Funktionsstörungen kommen. Wenn eine gleichzeitige Verwendung notwendig ist, solltest du den Sensor und die anderen Geräte immer im Blick behalten. Kontrolliere, ob dein Sensor und die anderen Geräte ordnungsgemäß funktionieren.
Tragbare Hochfrequenz-Kommunikationsgeräte (einschließlich Peripheriegeräte wie Antennenkabel und externe Antennen) dürfen nur in einem Abstand von mindestens 30 cm zum Sensor betrieben werden. Anderenfalls können sie die Leistung des Sensors beeinträchtigen.
Elektromagnetische Emissionen
Der Sensor erfüllt die folgenden Emissionsnormen.
HF-Störaussendungen nach:
- CISPR 11 (EN 55011) Klasse B, Gruppe 1
- RTCA DO160G Abschnitt 21, Kategorie M zur Verwendung im Fahrgastraum
Elektromagnetische Störfestigkeit
Der Sensor erfüllt die folgenden Normen für Störfestigkeit und Pegel für die Prüfung der Störfestigkeit.
Elektrostatische Entladung (IEC 61000-4-2), Prüfpegel:
- Kontakt: ±2 kV, ±4 kV, ±6 kV, ±8 kV
- Luft: ±2 kV, ±4 kV, ±8 kV, ±15 kV
Abgestrahlte elektromagnetische HF-Felder (IEC 61000-4-3), Prüfpegel:
- 10 V/m, 80 MHz–2,7 GHz, 80 % AM bei 1 kHz
Nahfeld drahtloser HF-Kommunikationsgeräte (IEC 60601-1-2 Tabelle 9), Prüfpegel:
Prüffrequenz | Band a) | Dienst a) | Modulation | PEGEL FÜR DIE PRÜFUNG DER STÖRFESTIGKEIT |
|---|---|---|---|---|
385 | 380 bis 390 | TETRA 400 | Pulsmodulation b) | 27 |
450 | 430 bis 470 | GMRS 460, FRS 460 | FM c) | 28 |
710 | 704 bis 787 | LTE-Band 13, 17 | Pulsmodulation b) | 9 |
745 | ||||
780 | ||||
810 | 800 bis 960 | GSM 800/900, TETRA 800, iDEN 820, CDMA 850, LTE-Band 5 | Pulsmodulation b) | 28 |
870 | ||||
930 | ||||
1720 | 1700 bis 1990 | GSM 1800; CDMA 1900; GSM 1900; DECT; LTE-Band 1, 3, 4, 25; UMTS | Pulsmodulation b) | 28 |
1845 | ||||
1970 | ||||
2450 | 2400 bis 2570 | Bluetooth, WLAN, 802.11 b/g/n, RFID 2450, LTE-Band 7 | Pulsmodulation b) | 28 |
5240 | 5100 bis 5800 | WLAN 802.11 a/n | Pulsmodulation b) | 9 |
5500 | ||||
5785 | ||||
Wenn dies zum Erreichen des PEGELS FÜR DIE PRÜFUNG DER STÖRFESTIGKEIT erforderlich ist, kann der Abstand zwischen der Sendeantenne und dem MEDIZINISCHEN ELEKTRISCHEN GERÄT bzw. SYSTEM auf 1 m verringert werden. Der Prüfabstand von 1 m ist gemäß IEC 61000-4-3 zulässig. | ||||
a) Bei einigen Diensten sind nur die Uplink-Frequenzen enthalten. b) Der Träger muss mit einem Rechtecksignal mit einem Tastgrad von 50 % moduliert werden. c) Als Alternative zur FM-Modulation kann der Träger auch anhand eines Rechtecksignals mit einem Tastgrad von 50 % bei 18 Hz pulsmoduliert werden. Auch wenn es sich hierbei nicht um eine tatsächliche Modulation handelt, wäre dies der ungünstigste Fall. | ||||
Magnetfelder mit energietechnischen Frequenzen (IEC 61000-4-8), Prüfpegel:
- 30 A/m, 50 Hz
- 30 A/m, 60 Hz
Magnetische Nahfelder (IEC 61000-4-39), Prüfpegel:
- 8 A/m, 30 kHz, CW-Modulation
- 65 A/m, 134,2 kHz, pulsmoduliert, Tastgrad 50 %, 2,1 kHz Wiederholrate
- 7,5 A/m, 13,56 MHz, pulsmoduliert, Tastgrad 50 %, 50 kHz Wiederholrate
Schutz vor elektrischem Schlag
Gerätetyp BF nach Norm IEC 60601-1. Schutz vor elektrischem Schlag.
Schutz vor dem Eindringen von Flüssigkeiten
IP28: Der Sensor ist vor den Folgen von dauerhaftem Untertauchen in Wasser bis zu 1 Meter Tiefe für bis zu 60 Minuten geschützt.
Sterilisationsverfahren
Bestrahlung
Störsubstanzen
Die Einnahme der folgenden Störsubstanzen beim Tragen des Sensors kann dazu führen, dass fälschlicherweise erhöhte CGM-Werte in der App angezeigt werden:
- Ascorbinsäure (Vitamin C): über 500 mg täglich bei oraler Einnahme und grundsätzlich bei intravenöser Gabe
- Nahrungsergänzungsmittel mit Gentisinsäure
- Methyldopa
Wenn fälschlicherweise erhöhte CGM-Werte ausgegeben werden, kann es zu einer Überdosierung von Insulin kommen und/oder dazu, dass du eine Episode mit sehr niedrigen Glukosewerten verpasst. Falls du eine oder mehrere der aufgeführten Störsubstanzen einnimmst, wende dich bitte an dein medizinisches Fachpersonal.
Umgebungsbedingungen
Transport- und Lagerbedingungen für den Sensor in der ungeöffneten Verpackung:
- Temperaturbereich: 2 bis 27 °C
- Relative Luftfeuchtigkeit: 10 bis 90 % (ohne Kondensation)
- Umgebungsluftdruck: 549 bis 1.060 hPa
Es dürfen nur ungeöffnete Produkte gelagert werden. Führe den Sensor unmittelbar nach dem Öffnen der Packung ein.
Betriebsbedingungen für den Sensor:
- Temperaturbereich: 10 bis 40 °C
- Relative Luftfeuchtigkeit: 15 bis 90 % (ohne Kondensation, Wasserdampfpartialdruck von weniger als 50 hPa)
- Umgebungsluftdruck: 700 bis 1.060 hPa
- Maximale Höhe: 3.000 m
Die Aufwärmphase des CGM-Geräts von der niedrigsten zulässigen Lagertemperatur (2 °C) bis zur niedrigsten zulässigen Betriebstemperatur (10 °C) dauert weniger als 17 Minuten.
Die Oberflächentemperatur des Sensors bleibt unter 43 °C und überschreitet 41 °C nur für kurze Zeit.
Leistungsdaten
Besprich mit deinem medizinischen Fachpersonal, wie du mit den folgenden Daten umgehst.
Die Leistung des Accu-Chek SmartGuide Sensors wurde in einer kontrollierten klinischen Studie evaluiert (Daten liegen vor). Die Studie wurde in 3 Kliniken durchgeführt, und insgesamt nahmen 48 Personen (ab 18 Jahren) mit Typ-1-Diabetes oder insulinpflichtigem Typ-2-Diabetes teil. Jede an der Studie teilnehmende Person trug dabei über 14 Tage 3 Sensoren an der Rückseite der Oberarme. Während der Studie wurde an manchen Tagen der Glukosespiegel absichtlich beeinflusst und dann wurden Blutzuckermessungen mit Kapillarblut zum Erhalt von Vergleichswerten durchgeführt. In der Studie wurden drei unterschiedliche Sensor-Chargen untersucht.
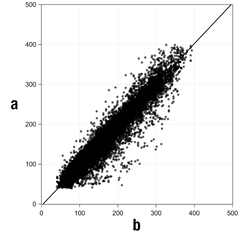
Abbildung 1: Regressionsanalyse der Sensorwerte im Vergleich zu den Kapillarmessungen
- Abbildung:
- a = CGM-Wert [mg/dL]; b = Vergleichswert [mg/dL]
Tabelle 1: Regressionsanalyse
Steigung | 1,02 |
Achsenabschnitt | -4,2 mg/dL (-0,2 mmol/L) |
Korrelation (Pearson’s r) | 0,96 |
N | 15993 |
Bereich | 40–400 mg/dL (2,2–22,2 mmol/L) |
MARD gesamt | 9,2 % |
Tabelle 2: Leistung des Sensors im Vergleich zu Kapillarmessungen bei verschiedenen Glukosebereichen
Glukose | MAD/MARD gesamt* |
|---|---|
< 54 mg/dL (3,0 mmol/L) | 7,5 mg/dL (0,42 mmol/L)* |
54–69 mg/dL (3,0–3,8 mmol/L) | 7,0 mg/dL (0,39 mmol/L)* |
70–180 mg/dL (3,9–10,0 mmol/L) | 9,8 % |
> 180–250 mg/dL (10,0–13,9 mmol/L) | 8,0 % |
> 250–350 mg/dL (13,9–19,4 mmol/L) | 7,3 % |
> 350 mg/dL (19,4 mmol/L) | 4,9 % |
* Bei Glukosewerten < 70 mg/dL (3,9 mmol/L) werden die Differenzwerte in mg/dL (mmol/L) statt relativen Werten (%) angegeben. | |
Die MARD (mittlere absolute relative Abweichung) ist der Mittelwert der absoluten relativen Abweichungen der CGM-Werte von den gleichzeitig gemessenen Blutzuckerwerten. Die MARD wird wie folgt bestimmt:
- Der gleichzeitig gemessene Blutzuckerwert wird vom kontinuierlich gemessenen Glukosewert subtrahiert. Der jeweilige absolute Differenzwert wird in Relation zum gemessenen Blutzuckerwert gesetzt und als Prozentwert ausgedrückt. Die Prozentwerte aller Wertpaare werden addiert und das Ergebnis wird durch die Anzahl der Wertpaare (n) dividiert.
Die MAD (mittlere absolute Abweichung) ist der Mittelwert der absoluten Abweichungen der CGM-Werte von den gleichzeitig gemessenen Blutzuckerwerten. Die MAD wird wie folgt bestimmt:
- Der gleichzeitig gemessene Blutzuckerwert wird vom kontinuierlich gemessenen Glukosewert subtrahiert und die absolute Differenz wird notiert. Die Differenzwerte aller Wertpaare werden addiert und das Ergebnis wird durch die Anzahl der Wertpaare (n) dividiert.
Tabelle 3: Leistung des Sensors im Vergleich zu Kapillarmessungen über die Tragezeit des Sensors
Anfang | Mitte | Ende | |
|---|---|---|---|
MARD gesamt | 8,3 % | 9,0 % | 10,8 % |
Tabelle 4: Leistung des Sensors gemäß Übereinstimmungsraten
Gesamt- | Innerhalb von ±15 mg/dL (±0,8 mmol/L) und ±15 % der Kapillar- | Innerhalb von ±20 mg/dL (±1,1 mmol/L) und ±20 % der Kapillar- | Innerhalb von ±30 mg/dL (±1,7 mmol/L) und ±30 % der Kapillar- | Innerhalb von ±40 mg/dL (±2,2 mmol/L) und ±40 % der Kapillar- | |
Sensorleistung gesamt | 15993 | 13345 (83,4 %) | 14471 (90,5 %) | 15510 (97,0 %) | 15803 (98,8 %) |
Sensorleistung bei < 70 mg/dL (3,9 mmol/L) | 1121 | 998 (89,0 %) | 1057 (94,3 %) | 1112 (99,2 %) | 1118 (99,7 %) |
Sensorleistung bei 70–180 mg/dL (3,9– | 9793 | 7923 (80,9 %) | 8718 (89,0 %) | 9444 (96,4 %) | 9660 (98,6 %) |
Sensorleistung bei > 180 mg/dL (10,0 mmol/L) | 5079 | 4424 (87,1 %) | 4696 (92,5 %) | 4954 (97,5 %) | 5025 (98,9 %) |
Bitte beachte, dass alle aufgeführten Leistungsdaten mit Sensoren im Therapiemodus erhoben wurden. In der beschriebenen Studie wurde mit Sensoren im Verlaufsmodus insgesamt eine mittlere absolute relative Abweichung (MARD) von 10,2 % erzielt. Entscheidungen zur Insulindosierung dürfen nur im Therapiemodus getroffen werden. Weitere Informationen dazu findest du im Kapitel Sensor kalibrieren.
Unerwünschte Ereignisse
Im Verlauf der Studie traten keine schwerwiegenden unerwünschten Ereignisse auf, weder in Bezug auf die Teilnehmer noch in Bezug auf das Gerät. Jedoch traten im Verlauf der Studie insgesamt 35 unerwünschte Ereignisse auf. Davon standen 15 tatsächlich oder potenziell mit dem Gerät in Verbindung. Alle dieser 15 unerwünschten Ereignisse betrafen Reaktionen an der Applikationsstelle, wie z. B. kurze Blutungen, Schmerzen, Hämatome, Rötungen, leichte Entzündungen oder Juckreiz.